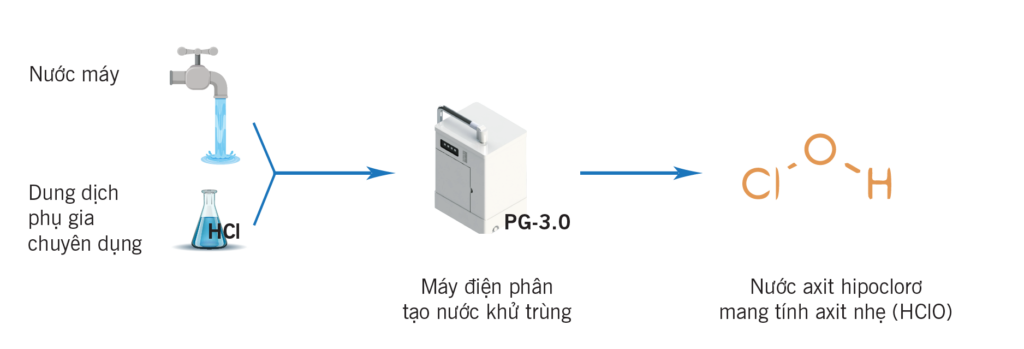
Axit Hypoclorơ
Danh pháp IUPAC : Axit Hypochlorous, axit chloric(I), chloranol, hydroxidoclo
Tên Khác : Hydrogen hypochlorite, clo hydroxide, nước điện phân, nước điện phân oxi hóa, nước kích hoạt điện
Số CAS : 7790-92-3
Khối lượng Phân tử : 52.46 g/mol
Công thức Phân tử : HCLO
Dạng : Dung dịch nước không màu
Độ hòa tan trong nước : Hòa tan
Tính axit : 7.53
Điện phân
Trong hóa học và sản xuất, điện phân là kỹ thuật sử dụng dòng điện một chiều trực tiếp để điều khiển phản ứng hóa học không tức thời. Điện phân là bước thương mại quan trọng trong việc tách các nguyên tố từ các nguồn có sẵn trong tự nhiên. Điện phân natri clorit (NaCl) và nước (H2O) để tạo ra axit hypochlorous. Công nghệ điện phân được Michael Farraday giải thích lần đầu tiên khi ông phát triển Định luật Điện phân vào những năm 1830. Tiến hành đưa dòng điện qua hai cực của dung dịch muối để tạo ra khí clo, natri hypoclorit (chất tẩy hoặc NaOCl), axit hypoclorơ , natri hiđroxit (NaOH), khí hiđrô (H2), khí ô-zôn (ozone), và các dấu vết của các chất oxi hóa mới.
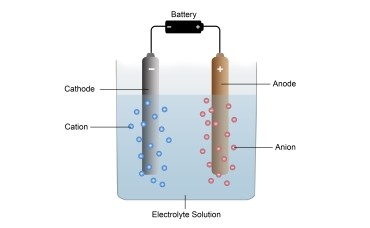
Qua trình cốt lõi của điện phân là biến đổi các nguyên tố và ion bằng cách gỡ bỏ hoặc thêm vào các electron từ dòng điện bên ngoài. Điện áp được đặt vào thông qua cặp điện cực được nhúng vào chất điện phân. Mỗi điện cực hấp thu ion tích điện ngược dấu. Ion tích điện dương (cations) di chuyển về cathode (điện tích âm). Ion tích điện âm (anions) di chuyển về anode (điện tích dương). Trong hóa học, việc mất electron gọi là quá trình oxi hóa, ngược lại tăng electron gọi là quá trình khử.
Ví dụ, bước đầu tiên để tạo axit hypoclorơ là quá trình điện phân nước muối để tạo khí hydro và khí clo, sản phẩm là các chất khí. Sản phẩm dạng khí thoát ra dưới dạng bong bóng từ chất điện phân và được thu lại.
2 NaCl(s) + 2 H20(l) → 2 NaOH(aq) + H2(g) + Cl2(g)
Công nghệ Màng Tế bào
Màng chuyển ion được tạo từ polymer chỉ cho phép các ion dương chạy qua. Có nghĩa là chỉ có ion natri từ dung dịch natri clo có thể chạy qua màng, và không phải ion clo. Ưu điểm của phương pháp này là dung dịch natri hydroxide được hình thành ở ngăn bên phải không bị nhiễm bẩn với dung dịch natri clorua bất kỳ. Dung dịch natri clorid được dùng phải tinh khiết. Nếu có chứa bất kỳ ion kim loại nào, những ion này sẽ đi qua màng và làm nhiễm bẩn dung dịch natri clorid.
Khí hydro được sản sinh ở cathode:
2H+(aq) + 2e- → H2(g)
Sodium hydroxide được sản sinh ở cathode:
Na+(aq) + OH-(aq) → NaOH(aq)
Chlorine được sản sinh ở anode :
2Cl-(aq) – 2e- → Cl2(g)
Nó bị nhiễm bẩn do khí oxi vì phản ứng:
4OH-(aq) – 4e- → 2H2O(l) + O2(g)
Bổ sung thêm clo vào nước cho ra axit hydrochloric (HCl) và axit hypoclorơ (HCLO):
Cl2(g) + H2O ⇌ HCLO(aq) + HCl(aq)
Cl2(g) + 4 OH− ⇌ 2 ClO-(aq) + 2 H2O(l) + 2 e−
Cl2(g) + 2 e− ⇌ 2 Cl-(aq)
Độ pH quyết định dạng clo tự do hiện diện trong dung dịch nước. Ở pH 5-6, dạng clo là gần 100% axit hypoclorơ (HCLO). Khi pH xuống 5, nó bắt đầu chuyển thành khí Cl2 (khí clo). pH trên 6, nó bắt đầu chuyển thành ion hypoclorit (OCl-).
Axit hypoclorơ là axit yếu (pKa khoảng 7,5), nghĩa là nó phân ly thành khí hidro và ion hypoclorit được ghi trong phương trình: : HCLO ⇌ H+ + OCl-
Trong khoảng pH từ 6,5 đến 8,5, quá trình phân ly không hoàn toàn và cả HCLO và OCl- đều có mặt ở mức độ nhất định pH dưới 6,5, phân ly HCLO không xảy ra, trong khi đó pH trên 8,5, xảy ra phân ly hoàn toàn thành OCl- .
Vì hiệu quả diệt khuẩn của HCLO cao hơn OCl-, clo hóa ở pH thấp hơn được ưu tiên. Hiệu quả diệt khuẩn của axit hypoclorơ (HCLO) cao hơn hiệu quả diệt khuẩn của ion hypoclorit (OCl-). Phân bố các dạng clo giữa HCLO và OCl- do pH quyết định như đã thảo luận ở trên.
Vì HCLO chiếm ưu thế ở pH thấp, khử trùng bằng clo hiệu quả hơn ở mức pH thấp. Khi pH cao, OCl- chiếm ưu thế, làm giảm hiệu quả diệt trùng.
Vô hoạt Vi khuẩn
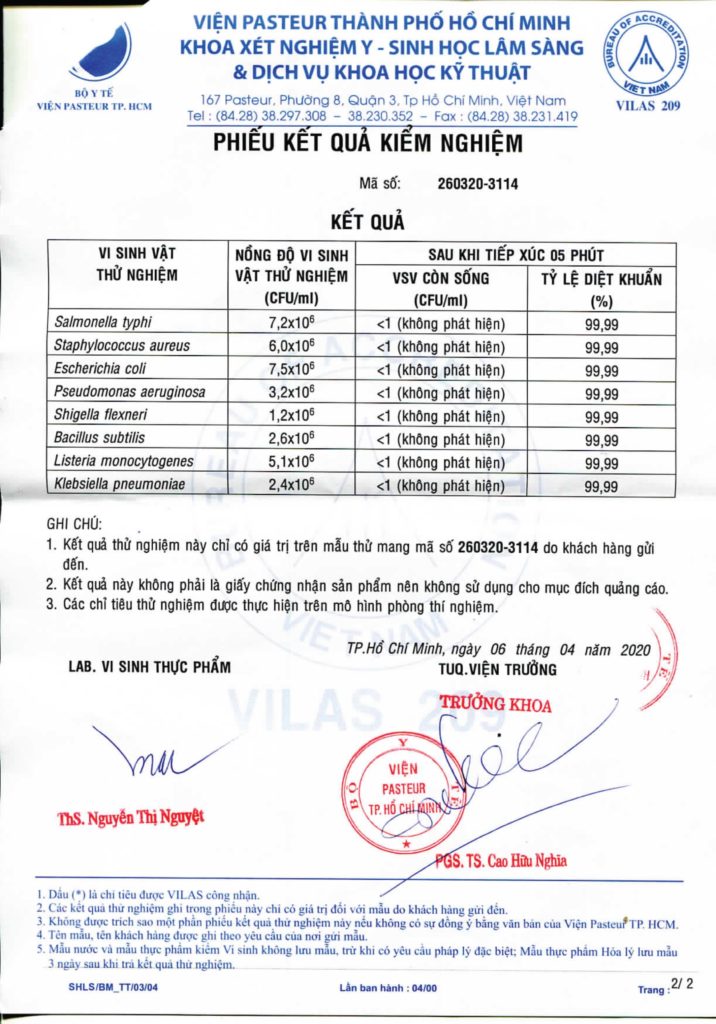
Chlorine là chất tẩy trùng cực kỳ hiệu quả để vô hoạt vi khuẩn Một nghiên cứu được tiến hành trong thập niên 1940 điều tra mức độ vô hoạt dưới dạng hàm số của thời gian đối với vi khuẩn E. coli, Pseudomonas aeruginosa, Salmonella typhi, và Shigella dysenteriae
(Butterfield et al., 1943). Kết quả nghiên cứu chỉ ra rằng HCLO hiệu quả hơn OCl- trong quá trình vô hoạt vi khuẩn Các kết quả này đã được một số nhà nghiên cứu xác nhận và kết luận rằng HCLO hiệu quả từ hơn từ 70 đến 80 lần so với OCl- trong quá trình vô hoạt vi khuẩn.
(Culp/Wesner/Culp, 1986). Kể từ năm 1986, có hàng trăm tài liệu được công bố xác nhận tính ưu việt của HCLO so với OCl-
(tham quan cơ sở dữ liệu nghiên cứu ).
Khó khăn lớn nhất là tạo ra axit hypoclorơ ở gần mức pH trung tính thay vì tạo ra khí clo hay hypoclorit và thực hiện ở dạng ổn định. axit hypoclorơ là phân tử giả bền. Phân tử này luôn muốn trở lại thành nước muối hoặc chuyển thành hypochlorite.
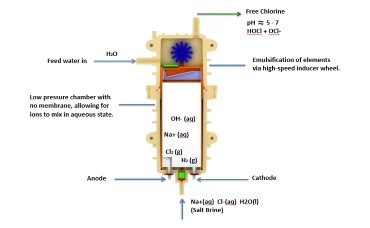
Công nghệ Tế Bào Đơn
Một trong những tiến bộ lớn nhất là sự phát triển của công nghệ Tế Bào Đơn trong đó dòng clo tự do đơn được tạo ra mà không có sản phẩm phụ là natri hydroxide (NaOH). Công nghệ này đã đưa đến sự phát triển các dung dịch axit hypoclorơ ổn định hơn và cho phép việc kiểm soát lớn hơn đối với pH của clo tự do được tạo ra. Vì độ pH của nước khác nhau tùy thuộc vào nguồn nước trên toàn thế giới, thay đổi độ pH của nước muối cho phép việc kiểm soát tốt hơn và nhất quán hơn trong quá trình tạo dung dịch clo tự do giữa pH 5 và pH 7 với ưu thế của axit hypoclorơ (HCLO).
Phản ứng Anode :
2Cl-(l) → Cl2(g) + 2e-
Phản ứng Cathode :
2H2O(l) + 2e- → H2(g) + 2OH- (aq)
Tạo ra Chlorine Tự do :
Cl2 (g) + H2O → HCLO + HCl
Cl2 (g) + 2OH-(aq) → OCl- (aq) + Cl-(aq) + H2O(l)